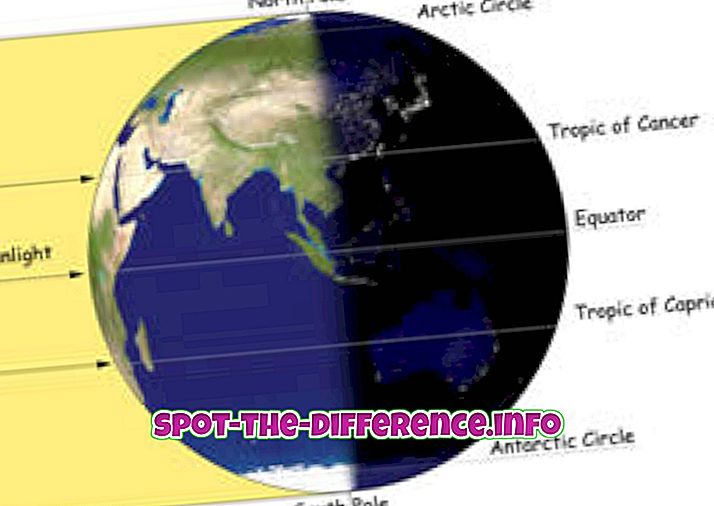
Diferencia clave: la masa atómica es simplemente la masa de un isótopo específico, o la masa combinada de los protones, neutrones y electrones del átomo. El número atómico es el número de protones que se encuentran en el núcleo de un elemento.
Enfrentémoslo: la química es confusa, la cantidad de elementos, números atómicos, enlaces, masa, peso, átomos, etc. Todas estas palabras comienzan a confundirse después de un cierto tiempo que una persona ya no puede distinguir una de la otra. Bien, masa atómica y número atómico son dos de esas palabras que a menudo se confunden y usan indistintamente.
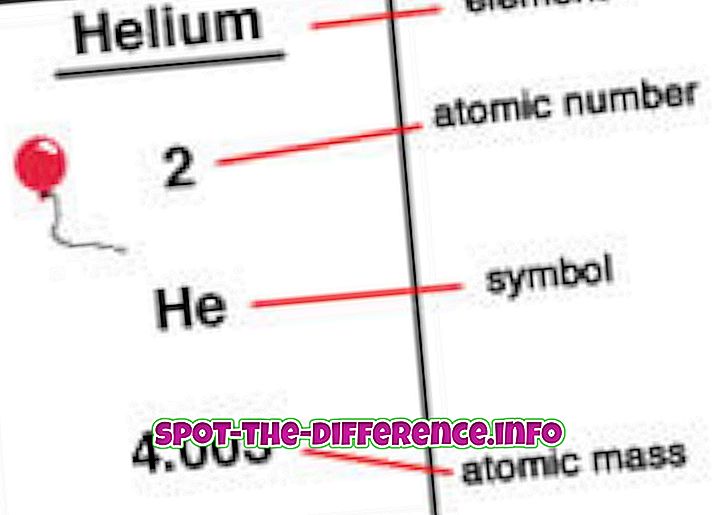
La masa atómica es la masa de un átomo cuando está en reposo. Esto se debe a que cuando un átomo se mueve a una velocidad muy alta, tiende a aumentar en masa. Aunque según la definición, la masa atómica es la masa de todos los protones, neutrones y electrones, los electrones son demasiado pequeños para hacer una diferencia significativa en la masa atómica. La mayoría de los elementos en la tabla periódica tienen isótopos y, debido a la diferencia en el recuento de neutrones, la masa de cada isótopo también cambia.
La masa atómica se expresa utilizando unidades de masa atómica o amu. Una unidad de masa atómica es igual a 1/12 de la masa de carbono-12. Cuando la masa de un átomo se divide por 1/12 de la masa de Carbono-12, se obtiene la masa relativa del elemento. Sin embargo, la masa relativa de un objeto es en realidad el peso atómico de un elemento, ya que se calcula considerando todos los isótopos. Sin embargo, esto no debe asumirse como masa atómica de un elemento.

El número atómico es el número de protones que se encuentran en el núcleo de un elemento. Cuando un átomo es neutral, significa que tiene el mismo número de protones y electrones. El número atómico se indica con una Z. Dado que cada elemento tiene un número diferente de protones, este número también se usa para representar un elemento. Los isótopos generalmente comparten el mismo número atómico pero se clasifican usando su masa atómica, por ejemplo, Carbono-12, Carbono-13.
Los elementos se colocan en orden de número atómico en una tabla periódica. El número atómico aparece en la esquina superior izquierda del elemento como superíndice. Los números atómicos pueden ayudar a divulgar información sobre el elemento y muchas personas pueden ver el número atómico e indicar qué elemento es. También indica dónde se puede colocar en la tabla periódica y si es líquido, gas o sólido. El número atómico también proporciona información sobre la carga del núcleo, los estados de oxidación, el comportamiento de enlace, la carga del ion, etc.