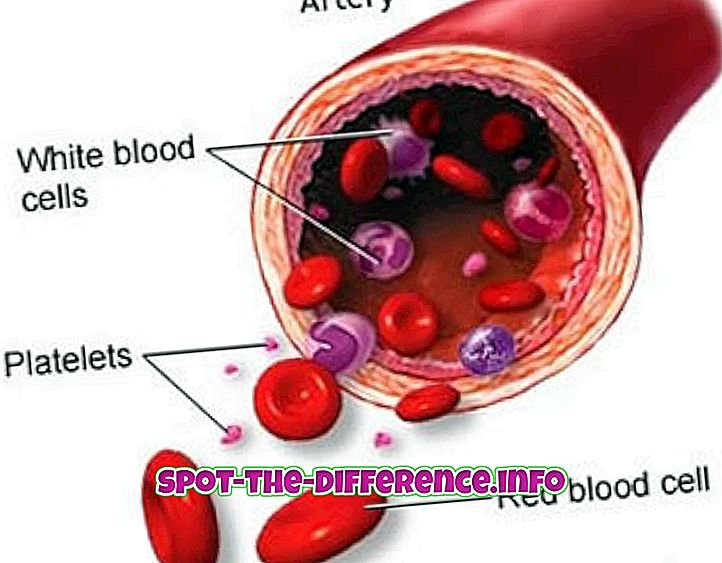
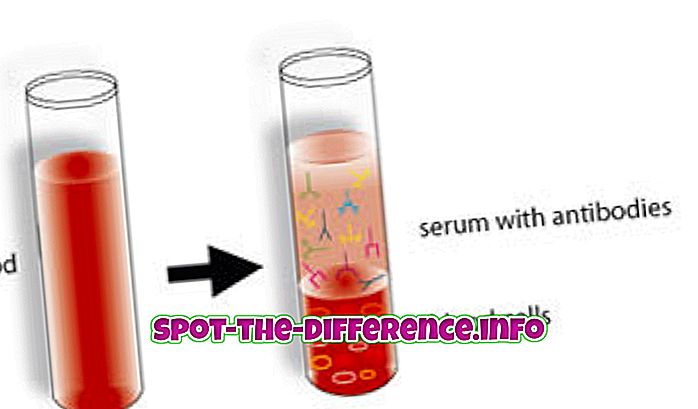
Diferencia clave: la absorción es un fenómeno generalizado en el que un absorbente penetra completamente en el cuerpo de un sólido o líquido para formar un compuesto o una solución. Por otro lado, la adsorción es un fenómeno de superficie en el que las moléculas de un adsorbato se concentran solo en la superficie de un adsorbente.
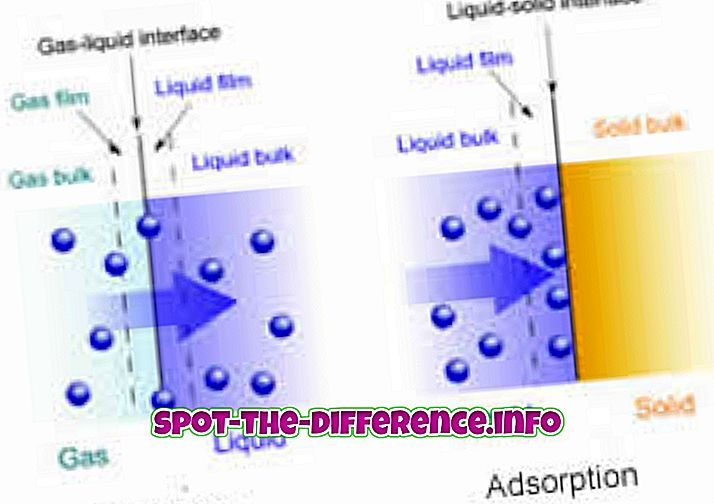
Reacción química: dióxido de carbono absorbido por una solución de carbono potásico
Proceso físico - Aire absorbido en agua por disolución.

Hay dos tipos de modos de adsorción: químicos y físicos. En la adsorción química, las moléculas y la superficie están unidas por fuerzas débiles de Vander Walls. Por otro lado, en la adsorción química, se forma un enlace químico entre las moléculas y la superficie.
Por lo tanto, la diferencia principal entre la adsorción y la absorción es que la absorción es un fenómeno general, lo que significa que ocurre en todo el cuerpo del material, mientras que la adsorción sigue siendo un fenómeno de la superficie. La adsorción es siempre exotérmica, mientras que la absorción es endotérmica. La sorción incluye ambos procesos de absorción y adsorción.
Comparación entre la adsorción y la absorción:
Adsorción | Absorción | |
Definición | Acumulación de un soluto de gas o líquido en la superficie de un sólido o un líquido. | Difusión de una sustancia en un líquido o sólido para formar una solución o compuesto |
Ejemplo | Los gases inertes se adsorben sobre el carbón vegetal. | Una esponja seca absorbe el agua. |
De intercambio de calor | Exotérmica con excepción de la adsorción de H2 sobre vidrio. | Endotérmico |
Alcanzando el equilibrio | Comparativamente mas rapido | Comparativamente lento |
Concentración | La concentración en la superficie del adsorbente es diferente a la del volumen | La concentración permanece igual en todo el material. |
Tasa de ocurrencia | Inicialmente es rápido pero luego su tasa comienza a disminuir. | Se lleva a cabo a ritmo uniforme. |