Diferencia clave: la molaridad, también conocida como concentración molar, mide el número de moles de una sustancia presente por litro de solución. La molaridad se denota con una M. mayúscula. La molalidad mide el número de moles de una sustancia presente por kilogramo de solvente. La molalidad se denota con una m minúscula.
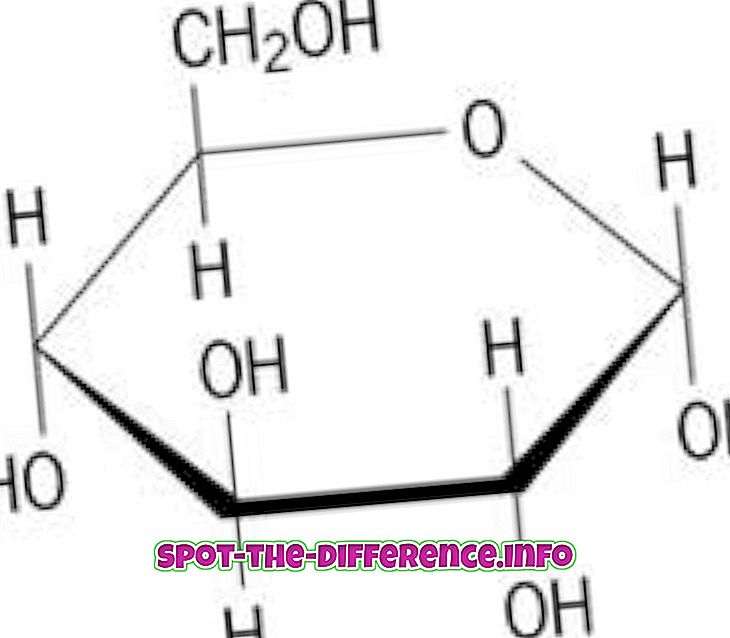
Ambos conceptos basan sus cálculos en la cantidad de moles presentes en la solución actual. Una solución puede definirse como una mezcla homogénea, lo que significa que dos o más componentes se han mezclado hasta el punto de que no se puede distinguir a simple vista. Estos dos conceptos requieren la comprensión de los lunares, ya que determina la cantidad de moles presentes en la solución. La teoría de los lunares fue descubierta por el científico italiano Amedeo Avogardo.
En 1811, Avogardo propuso que el volumen de gas, a una temperatura y presión dadas, es proporcional al número de átomos o moléculas independientemente de su naturaleza. Este concepto es conocido como la constante de Avogardo. Se define como el número de partículas constituyentes (generalmente átomos o moléculas) en un mol de una sustancia dada. En términos laicos, un mol de una sustancia representaría el número de átomos y moléculas presentes en el elemento. Por ejemplo: el oxígeno tiene un peso atómico de 16, esto representaría la masa de por mol de oxígeno. Entonces, un mol de oxígeno tendría una masa de 16 gramos. Según Avogardo, un mol de oxígeno tendría la misma cantidad de átomos que un mol de hidrógeno. Sin embargo, pueden diferir en peso.
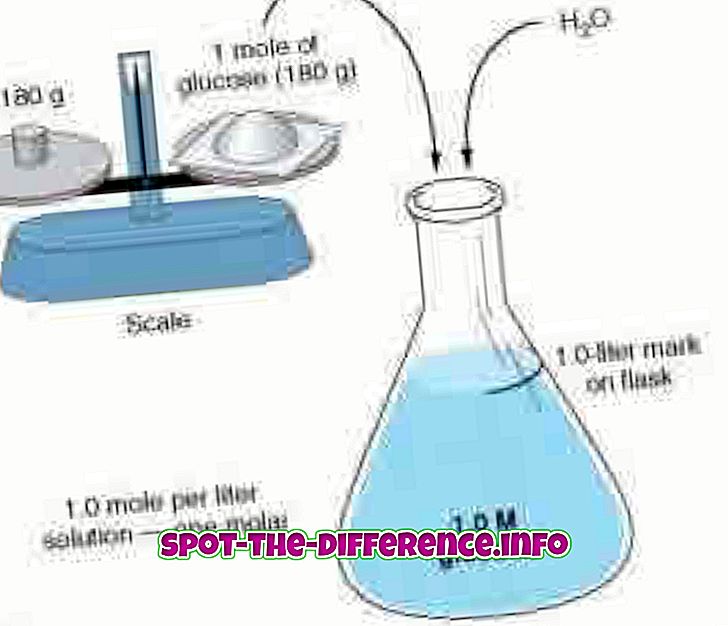
La molaridad y la molalidad miden la concentración utilizando dos enfoques diferentes. La molaridad, también conocida como concentración molar, mide el número de moles de una sustancia presente por litro de solución. La molaridad se denota con una M mayúscula. Por lo tanto, una solución con 1.0M indicaría que contiene 1 mol de soluto por litro de solución. Por ejemplo: Una solución de agua y azúcar. Si la solución se mide como 1.0 M, entonces la solución tiene 1 mol de azúcar por litro de solución presente. La molaridad también se conoce como concentración de cantidad de sustancia, concentración de cantidad, concentración de sustancia o simplemente concentración. La molaridad se puede calcular mediante la fórmula: M = mol (número de moles) / L (volumen de solución en litros).

La molalidad mide el número de moles de una sustancia presente en cada kilogramo de solvente. La molalidad se denota con una m minúscula. Por lo tanto, una solución con 1, 0 m indicaría que contiene 1 mol de soluto por kilogramo de solvente. Diferenciemos el soluto del solvente. El soluto es la sustancia que se disuelve en otra sustancia. Un solvente es una sustancia que disuelve el soluto. Entonces, si el agua y el azúcar se mezclan, el azúcar sería el soluto y el disolvente el agua. El agua mezclada con azúcar sería la solución. Ahora, en la molalidad, es de suma importancia que los lunares se dividan por la masa del disolvente y no por la solución. La molalidad se puede calcular mediante la fórmula: m = mol (número de moles) / KG (masa de disolvente en kg).
¿Por qué la diferencia? Bueno, ambos se utilizan cuando se trata de la temperatura. Si una solución cambia de temperatura, se utiliza la molalidad. Pero para soluciones que se mantendrán a temperatura constante se usa la molaridad. Esto se debe a que a medida que la temperatura aumenta o disminuye, el volumen de la solución cambia y esto afecta directamente la molaridad. Por lo tanto, la molalidad se utiliza para calcular la concentración.