Diferencia clave: la difusión es el proceso mediante el cual las moléculas se mueven y viajan de un lugar a otro sin requerir un movimiento masivo. La efusión es el proceso por el cual las moléculas viajan a través de un orificio desde un lugar de alta concentración a baja concentración.
Los términos difusión y derrame se usan comúnmente en muchas ciencias, como la química, la física y la biología. En química estos dos términos son dos propiedades de los gases. Estos dos son confusos para muchas personas que están aprendiendo los conceptos básicos de los gases y sus propiedades. Difusión y Efusión son dos términos diferentes que significan dos cosas diferentes y no deben usarse indistintamente. La difusión se refiere a la capacidad de los gases para mezclarse entre sí, mientras que la efusión se refiere a la capacidad de los gases para viajar a través de un pequeño orificio. La difusión también se utiliza en sociología, economía y finanzas para referirse a la difusión de personas, ideas y valores.
La difusión es el proceso por el cual las moléculas se mueven y viajan de un lugar a otro sin requerir un movimiento masivo. La difusión hace que las moléculas se muevan o se mezclen utilizando solo energía cinética. La palabra "difusión" se deriva de la palabra latina "diffundere" que significa "extenderse". En la difusión, las moléculas están en un estado constante de movimiento y cuando son impulsadas por energía cinética o térmica, tienden a mezclarse con otras moléculas dando como resultado una mezcla inseparable. Tomemos un enfoque práctico, un contenedor se divide en secciones A y B utilizando una partición sólida; la primera sección está llena de agua, mientras que la segunda sección está llena de tinte rojo. Ahora, cuando se levanta la partición, el tinte y el agua intentan llenar todo el contenedor. Luego el tinte mancha lentamente el agua de color rojo, siendo esta la difusión.
La difusión hace que las moléculas se desplacen de un área de mayor concentración a un área de menor concentración, dando como resultado la mezcla de todas las moléculas. La difusión se detiene cuando todas las moléculas se distribuyen uniformemente. La difusión no se limita al agua y funciona mejor en estados gaseosos, donde las moléculas tienen más energía y capacidad para mezclarse con otras moléculas. Hay dos enfoques para la difusión: fenomenológico y atomístico. Según el enfoque fenomenológico, las moléculas viajan desde regiones de mayor concentración a regiones de menor concentración. En el enfoque atomístico, se considera que la difusión ocurre debido al desplazamiento aleatorio de las partículas de difusión, en el que la difusión es impulsada por la energía térmica, lo que hace que se mezclen. La difusión juega un papel importante en la creación de minerales, nutrientes y energía que son requeridos por el cuerpo.

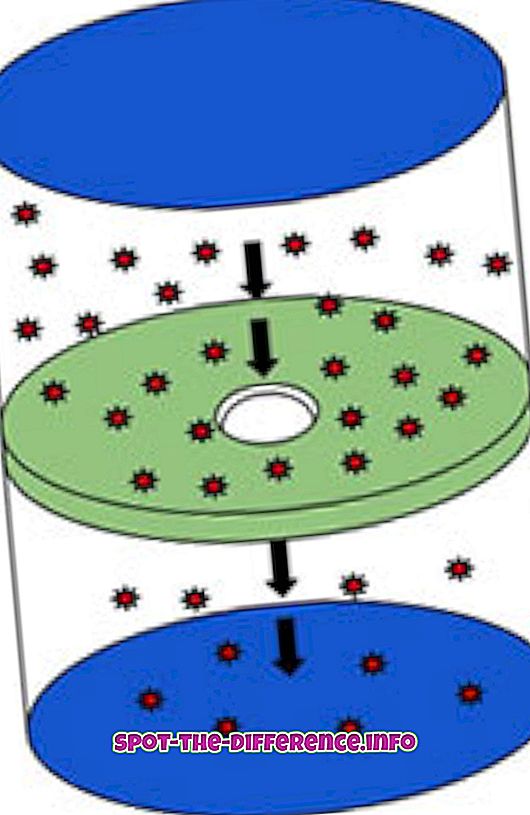
La efusión es el proceso por el cual las moléculas viajan a través de un orificio desde un lugar de alta concentración a baja concentración. El proceso describe la capacidad del gas para viajar a través de un pequeño agujero sin colisiones entre moléculas. Esto ocurre cuando el diámetro del agujero es considerablemente más pequeño que el recorrido libre medio de las moléculas. La trayectoria libre media es la distancia promedio recorrida por una partícula en movimiento entre colisiones sucesivas. Un ejemplo práctico de esto sería llenar un contenedor de una botella con humo y hacer un pequeño agujero en la botella, el humo que comienza a extraerse de los agujeros se considera un derrame.
De acuerdo con el químico escocés Thomas Graham, quien creó la fórmula para medir el derrame, creó una Ley Graham que determina qué tan rápido viajará el gas y cómo se puede medir. De acuerdo con la Ley de Graham, la velocidad a la que se emiten los gases depende de su peso molecular. El gas con un peso molecular más bajo se difundirá más rápidamente que un gas con un peso molecular más alto. La efusión se calcula midiendo cuántas moléculas pasan a través del agujero en un segundo. De manera similar, en termodinámica, la velocidad de derrame de un gas es inversamente proporcional a la raíz cuadrada de la masa de sus partículas.